7月,華中科技大學同濟醫學院附屬同濟醫院的馬丁院士、高慶蕾教授及方勇教授攜手美國德克薩斯大學M.D.Anderson癌癥中心的梁晗教授團隊,在頂尖科學期刊《Cell》上發表了關于卵巢癌治療的重要研究成果,題為《卵巢癌新輔助PARP抑制劑或化療揭示同源重組缺陷型腫瘤治療新靶點——eTreg細胞》。

背景
該研究聚焦于高致死率的高漿卵巢癌,此類卵巢癌占所有卵巢癌病例的七成,當前標準療法——鉑類新輔助化療雖初期響應良好,但易產生耐藥性,導致五年生存率長期徘徊在30%,患者預后亟需改善。
靶點介紹
作為婦科腫瘤領域的一項突破性貢獻,該研究通過前瞻性臨床試驗與多組學深度分析,首次闡明了同源重組修復缺陷(HRD)與無缺陷(HRP)卵巢癌在腫瘤微環境特征上的顯著差異。研究不僅驗證了口服PARP抑制劑尼拉帕利在高級別漿液性卵巢癌治療中的顯著療效及其作為新輔助治療策略的潛力,還創新性地提出了尼拉帕利聯合CCR8單抗,以清除eTreg細胞為策略的新型免疫治療方案,針對HRD腫瘤。
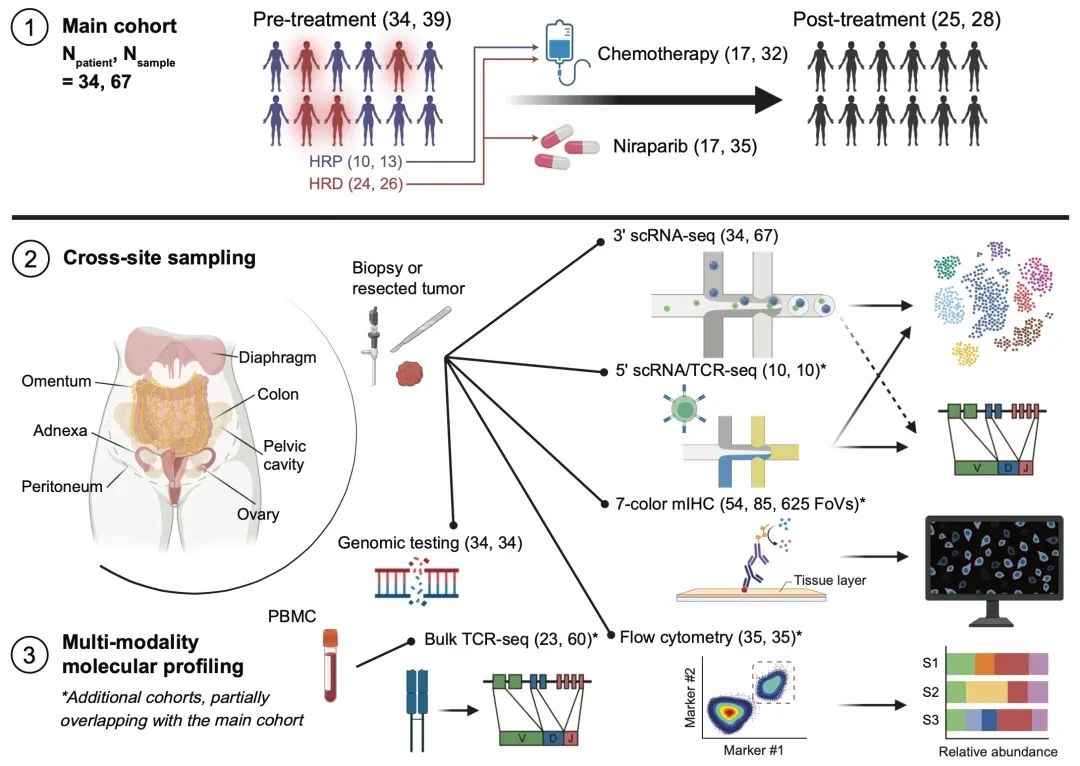
依托NANT臨床試驗的豐富資源,研究團隊系統收集了尼拉帕利單藥及含鉑化療前后的卵巢癌組織與血液樣本,結合臨床HRD檢測、單細胞轉錄組測序、T淋巴細胞受體序列分析以及先進的免疫組化與流式細胞術技術,揭示了以下關鍵發現:
1. HRD陽性卵巢癌的免疫微環境更為活躍,特別是增殖型及IFN反應性CD4/8+T淋巴細胞比例顯著增加。
2. IFN反應性腫瘤細胞比例與eTreg細胞比例呈正相關,這一機制與腫瘤細胞內IFN-MHCⅡ通路的激活緊密相關。
3. HRD陽性腫瘤受到eTreg細胞的負向調控,而尼拉帕利及鉑類化療藥物均能有效逆轉此調控,進而減輕腫瘤負荷(表現為CA125水平下降)。
展望與總結
歷經四年不懈探索,研究團隊通過大規模的單細胞測序與靶點篩選,成功鎖定了eTreg這一全新治療靶點。高慶蕾教授強調,這一發現不僅標志著卵巢癌靶向免疫治療的新紀元,也為精準醫療在卵巢癌治療中的應用開辟了廣闊前景。
尤為值得一提的是,此次研究成果的發表,首次以漢字形式出現在《CELL》雜志,彰顯了中國科學家在全球科研舞臺上的重要影響力與貢獻。
文獻來源:https://www.cell.com/cell/fulltext/S0092-8674(24)00653-6



